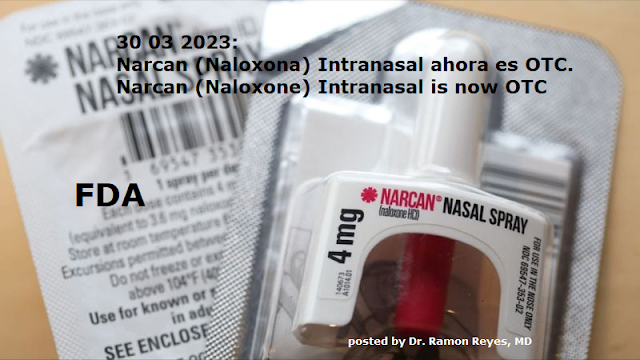
This shelf-life extension applies only to NARCAN (4 mg) nasal spray products produced following today.
This action was taken to prevent overdoses and reduce overdose-related deaths by expanding access to naloxone and other overdose reversal agents.
La FDA aprueba el primer aerosol nasal de naloxona de venta libre
La agencia continúa tomando medidas críticas para reducir las muertes por sobredosis de drogas provocadas principalmente por opioides ilícitos
March 29, 2023
English
Hoy, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés) aprobó Narcan, un aerosol nasal de clorhidrato de naloxona de 4 miligramos (mg), para uso de venta libre, sin receta médica; es el primer producto de naloxona aprobado para su uso sin prescripción. La naloxona es un medicamento que revierte rápidamente los efectos de una sobredosis de opioides y es el tratamiento acostumbrado para la sobredosis de opioides. La acción de hoy cimienta el camino para que este medicamento que salva vidas revierta una sobredosis de opioides y se venda directamente a los consumidores en lugares como farmacias, tiendas de conveniencia, supermercados y gasolineras, así como en línea.
El plazo para la disponibilidad y el precio de este producto de venta libre lo determina el fabricante. La FDA trabajará con todas las partes interesadas para ayudar a facilitar la disponibilidad constante de productos de aerosol nasal de naloxona durante el tiempo necesario para efectuar el cambio de que Narcan pase a ser un medicamento que requiere receta médica a uno de venta libre, lo que puede tardar meses. Otras formulaciones y dosis de naloxona permanecerán disponibles solo con receta médica.
La sobredosis de drogas persiste como un importante problema de salud pública en los Estados Unidos, con más de 101,750 sobredosis fatales reportadas que ocurrieron en el período de 12 meses que finalizó en octubre de 2022, causadas principalmente por opioides sintéticos como el fentanilo ilícito.
“La FDA mantiene su compromiso de ocuparse de las complejidades cambiantes de la crisis de sobredosis. Como parte de este trabajo, la agencia ha utilizado su autoridad normativa para facilitar un mayor acceso a la naloxona al alentar el desarrollo y la aprobación de un producto de naloxona de venta libre para responder a la urgente necesidad de salud pública”, afirmó el comisionado de la FDA, el doctor Robert M. Califf. “La aprobación de hoy del aerosol nasal de naloxona de venta libre ayudará a mejorar el acceso a la naloxona, aumentará la cantidad de lugares donde está disponible y ayudará a reducir las muertes por sobredosis de opioides en todo el país. Animamos al fabricante a que priorice la accesibilidad al producto, haciéndolo disponible lo antes posible y a un precio accesible”.
El aerosol nasal Narcan fue aprobado por primera vez por la FDA en 2015 como medicamento recetado. De acuerdo con un proceso para cambiar el estado de un medicamento de venta con receta a venta sin receta, el fabricante proporcionó datos que demuestran que el medicamento es seguro y eficaz para su uso según las indicaciones de la etiqueta propuesta. El fabricante también demostró que los consumidores pueden entender cómo usar el medicamento de manera segura y eficaz sin la supervisión de un profesional de la salud. La solicitud para aprobar el aerosol nasal Narcan para uso de venta libre recibió el estado de revisión prioritaria y fue objeto de una reunión del comité asesor en febrero de 2023, donde los miembros del comité votaron unánimemente para recomendar que se aprobara para su comercialización sin receta.
La aprobación del aerosol nasal Narcan de venta libre requerirá un cambio en la etiqueta de los productos genéricos de aerosol nasal de naloxona de 4 mg actualmente aprobados que dependen de Narcan como su producto farmacéutico de referencia. Los fabricantes de estos productos deberán presentar un complemento a sus solicitudes para cambiar efectivamente sus productos al estado de venta libre. La aprobación también puede afectar el estado de otras marcas de aerosol nasal de naloxona de 4 mg o inferior, pero las determinaciones se realizarán caso por caso y la FDA puede comunicarse con otras empresas según sea necesario.
El uso del aerosol nasal Narcan en personas que son dependientes de los opioides puede provocar una abstinencia grave de los opioides caracterizada por dolores corporales, diarrea, aumento de la frecuencia cardíaca (taquicardia), fiebre, moqueo, estornudos, piel de gallina, sudoración, bostezos, náuseas o vómitos, nerviosismo, inquietud o irritabilidad, escalofríos o temblores, calambres abdominales, debilidad y aumento de la presión arterial.
“La naloxona es una herramienta clave para abordar las sobredosis de opioides y la aprobación de hoy destaca los amplios esfuerzos que la agencia ha realizado para combatir la crisis de sobredosis”, expresó la doctora Patrizia Cavazzoni, directora del Centro de Evaluación e Investigación de Medicamentos de la FDA. “La FDA trabaja con nuestros colaboradores federales a fin de garantizar el acceso continuo a naloxona en todas sus presentaciones durante la transición de este producto del estado de venta con receta al estado de venta sin receta a de venta libre. Además, trabajaremos con cualquier patrocinador que busque comercializar un producto de naloxona sin receta, incluso a través de un cambio de venta con receta a de venta libre, y exhortaremos a los fabricantes a comunicarse con la agencia lo antes posible para iniciar conversaciones”.
La FDA ha adoptado una serie de medidas para ayudar a facilitar el acceso a los productos de naloxona. En noviembre de 2022, la agencia anunció su evaluación preliminar de que ciertos productos de naloxona, como el que finalmente se aprobó hoy, tienen el potencial de ser seguros y eficaces para su uso sin receta y animó a los patrocinadores a presentar solicitudes. para la aprobación de productos de naloxona de venta libre. La agencia anunció previamente en 2019 que había diseñado, probado y validado un modelo de etiqueta de información del medicamento (DFL, por sus siglas en inglés) de naloxona con pictogramas fáciles de entender sobre cómo usar el medicamento para alentar a los fabricantes a buscar la aprobación de productos de naloxona de venta libre. La DFL modelo se utilizó para respaldar la solicitud aprobada junto con los resultados de un estudio de validación de factores humanos de uso simulado diseñado para evaluar si todos los componentes del producto con los que un usuario interactuaría podrían usarse de manera segura y eficaz según lo previsto.
A través del Marco de prevención de sobredosis de la FDA, la agencia sigue enfocada en responder a todas las facetas del consumo de sustancias, el consumo indebido, los trastornos por consumo de sustancias, las sobredosis y la muerte en los Estados Unidos. Las prioridades del marco incluyen: apoyar la prevención primaria al eliminar la exposición inicial innecesaria a medicamentos recetados y la prescripción prolongada inapropiada; fomentar la reducción de daños a través de la innovación y la educación; avanzar en el desarrollo de tratamientos basados en evidencia para los trastornos por consumo de sustancias; y proteger al público de medicamentos no aprobados, desviados o falsificados que presenten riesgos de sobredosis.
La FDA otorgó la aprobación de venta libre de Narcan a Emergent BioSolutions.
FDA Approves First Over-the-Counter Naloxone Nasal Spray
Agency Continues to Take Critical Steps to Reduce Drug Overdose Deaths Being Driven Primarily by Illicit Opioids
Read at FDA in english
Today, the U.S. Food and Drug Administration approved Narcan, 4 milligram (mg) naloxone hydrochloride nasal spray for over-the-counter (OTC), nonprescription, use – the first naloxone product approved for use without a prescription. Naloxone is a medication that rapidly reverses the effects of opioid overdose and is the standard treatment for opioid overdose. Today’s action paves the way for the life-saving medication to reverse an opioid overdose to be sold directly to consumers in places like drug stores, convenience stores, grocery stores and gas stations, as well as online.
The timeline for availability and price of this OTC product is determined by the manufacturer. The FDA will work with all stakeholders to help facilitate the continued availability of naloxone nasal spray products during the time needed to implement the Narcan switch from prescription to OTC status, which may take months. Other formulations and dosages of naloxone will remain available by prescription only.
Drug overdose persists as a major public health issue in the United States, with more than 101,750 reported fatal overdoses occurring in the 12-month period ending in October 2022, primarily driven by synthetic opioids like illicit fentanyl.
“The FDA remains committed to addressing the evolving complexities of the overdose crisis. As part of this work, the agency has used its regulatory authority to facilitate greater access to naloxone by encouraging the development of and approving an over-the-counter naloxone product to address the dire public health need,” said FDA Commissioner Robert M. Califf, M.D. “Today’s approval of OTC naloxone nasal spray will help improve access to naloxone, increase the number of locations where it’s available and help reduce opioid overdose deaths throughout the country. We encourage the manufacturer to make accessibility to the product a priority by making it available as soon as possible and at an affordable price.”
Narcan nasal spray was first approved by the FDA in 2015 as a prescription drug. In accordance with a process to change the status of a drug from prescription to nonprescription, the manufacturer provided data demonstrating that the drug is safe and effective for use as directed in its proposed labeling. The manufacturer also showed that consumers can understand how to use the drug safely and effectively without the supervision of a healthcare professional. The application to approve Narcan nasal spray for OTC use was granted priority review status and was the subject of an advisory committee meeting in February 2023, where committee members voted unanimously to recommend it be approved for marketing without a prescription.
The approval of OTC Narcan nasal spray will require a change in the labeling for the currently approved 4 mg generic naloxone nasal spray products that rely on Narcan as their reference listed drug product. Manufacturers of these products will be required to submit a supplement to their applications to effectively switch their products to OTC status. The approval may also affect the status of other brand-name naloxone nasal spray products of 4 mg or less, but determinations will be made on a case-by-case basis and the FDA may contact other firms as needed.
The use of Narcan nasal spray in individuals who are opioid dependent may result in severe opioid withdrawal characterized by body aches, diarrhea, increased heart rate (tachycardia), fever, runny nose, sneezing, goose bumps, sweating, yawning, nausea or vomiting, nervousness, restlessness or irritability, shivering or trembling, abdominal cramps, weakness and increased blood pressure.
“Naloxone is a critical tool in addressing opioid overdoses and today’s approval underscores the extensive efforts the agency has undertaken to combat the overdose crisis,” said Patrizia Cavazzoni, M.D., director of the FDA’s Center for Drug Evaluation and Research. “The FDA is working with our federal partners to help ensure continued access to all forms of naloxone during the transition of this product from prescription status to nonprescription/OTC status. Further, we will work with any sponsor seeking to market a nonprescription naloxone product, including through an Rx to OTC switch, and encourage manufacturers to contact the agency as early as possible to initiate discussions.”
The FDA has taken a series of measures to help facilitate access to naloxone products. In November 2022, the agency announced its preliminary assessment that certain naloxone products, such as the one ultimately approved today, have the potential to be safe and effective for over-the-counter use and encouraged sponsors to submit applications for approval of OTC naloxone products. The agency previously announced in 2019 that it had designed, tested, and validated a model naloxone Drug Facts Label (DFL) with easy-to-understand pictograms on how to use the drug to encourage manufacturers to pursue approval of OTC naloxone products. The model DFL was used to support the approved application along with the results of a simulated use Human Factors validation study designed to assess whether all the components of the product with which a user would interact could be used safely and effectively as intended.
Through the FDA Overdose Prevention Framework, the agency remains focused on responding to all facets of substance use, misuse, substance use disorders, overdose and death in the U.S. The framework’s priorities include: supporting primary prevention by eliminating unnecessary initial prescription drug exposure and inappropriate prolonged prescribing; encouraging harm reduction through innovation and education; advancing development of evidence-based treatments for substance use disorders; and protecting the public from unapproved, diverted or counterfeit drugs presenting overdose risks.
The FDA granted the OTC approval of Narcan to Emergent BioSolutions. https://www.fda.gov/news-events/press-announcements/fda-approves-first-over-counter-naloxone-nasal-spray
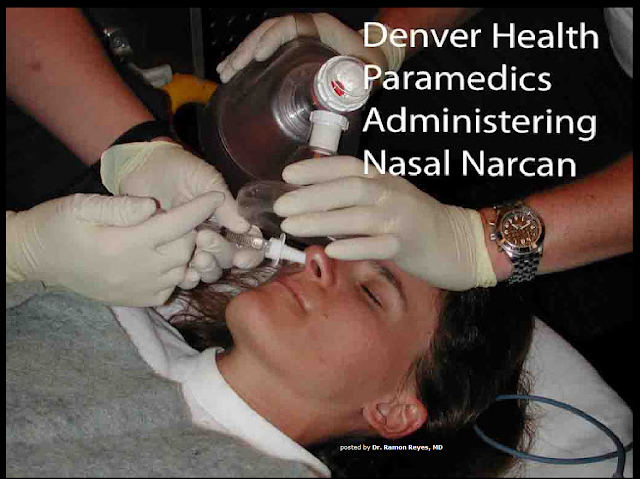
Study: New York EMTs Giving Intranasal Narcan Doses
Information from EMSWORLD
Until now, the drug overdose antidote was only administered by ALS providers.
Por favor compartir nuestras REDES SOCIALES @DrRamonReyesMD, así podremos llegar a mas personas y estos se beneficiarán de la disponibilidad de estos documentos, pdf, e-book, gratuitos y legales..
Grupo Biblioteca/PDFs gratis en Facebook
https://www.facebook.com/groups/PDFgratisMedicina #DrRamonReyesMD
https://www.facebook.com/DrRamonReyesMD
https://www.instagram.com/drramonreyesmd/
https://www.pinterest.es/DrRamonReyesMD/
https://twitter.com/eeiispain
Blog
http://emssolutionsint.blogspot.com/2016/12/dr-ramon-reyes-diaz-md-emt-t-dmo.html
TELEGRAM
Group https://t.me/joinchat/GRsTvEHYjNLP8yc6gPXQ9Q